- カテゴリ
まずは、前回の物理(熱力学)の解説から!
前回の問題 物理(熱力学)
<問題>
|
半径rの球形の容器の中に、ある単原子分子の希薄気体が封入されている。気体同士の衝突はなく、容器の壁と気体分子との衝突は完全弾性衝突とする。気体定数R、アボガドロ定数NA、気体分子の数N、容器の体積Vとして、以下の問いに答えよ。 (1)1個の分子(質量m、速度v)が容器の内壁に対して、球の中心と衝突点とを結ぶ線(法線)と角度θで衝突するとき、法線、接線方向それぞれの衝突前後の運動量変化を求めよ。 (2)1個の分子が単位時間に壁に衝突する回数を求めよ。 (3)全分子が単位時間に壁に与える力Fと圧力Pを求めよ。 (4)熱平衡でのエネルギー等分配則 <1/2·mvx2>=<1/2·mvy2>=<1/2·mvz2>=1/2·kT (k=R/NA) を用いて、理想気体の状態方程式を導け。但しTは絶対温度とする。 (5)窒素分子の分子量を28、R=8.31J/mol·Kとして、温度27℃の空気中における窒素分子の平均の速さを求めよ。 |
<ヒント>
(1)完全弾性衝突なので、エネルギーを失うことなくはね返る。したがって、面の接線方向は速度を変えず、法線方向の速度も大きさを変えずに、向きが逆なりはね返る。これは図を描くと分かると思います。
(2)1回衝突の間で気体分子が移動する距離を求めて、それを速度で割れば衝突時間になるので、その逆数を求めればよいです。
(3)力積と運動量の関係を考えましょう。
(4)(5)は(3)を利用します。
<解答>
この手の問題は、立方体の容器を用いることが多いですが、球体でもできるようにしておきましょう。パターンは同じで、1分子が1回に衝突する際の運動量変化、単位時間に衝突する回数を求め、そこから力積と運動量変化の関係から、単位時間に1分子、又は全分子が壁に及ぼす力、その力を面積で割ることで圧力を求め、エネルギー等分配則から理想気体の状態方程式を導く流れです。ボルツマン定数×アボガドロ数=気体定数の関係も知っておきましょう。
今週の問題 化学(有機化学)
<問題>
<ヒント>
(1)Aに付加した水素からA1分子中のC=C結合の数を求めましょう。
(2)Cは油脂を加水分解して得られ、粘性が高い液体であることから、その正体はグリセリンですね。
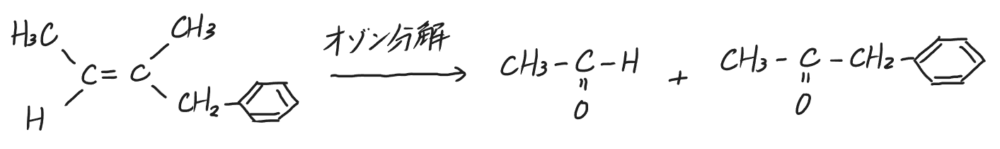
(3)(2)の結果から、Aはグリセリン1分子とD由来のカルボン酸2分子、E由来のカルボン酸1分子からなる化合物で、あとはDEの炭素の数を、銀鏡反応が無いことからCとDはギ酸ではないこと、又、EはベンズアルデヒトとFをオゾン分解で生じることから、Fはカルボキシル基をもつことが分かるので、Eは少なくとも炭素原子を9個もつこと、AとC(グリセリン)の炭素数から考えましょう。
学習や進路に対する質問等は、お気軽に問い合わせフォームからどうぞ。お待ちしています。