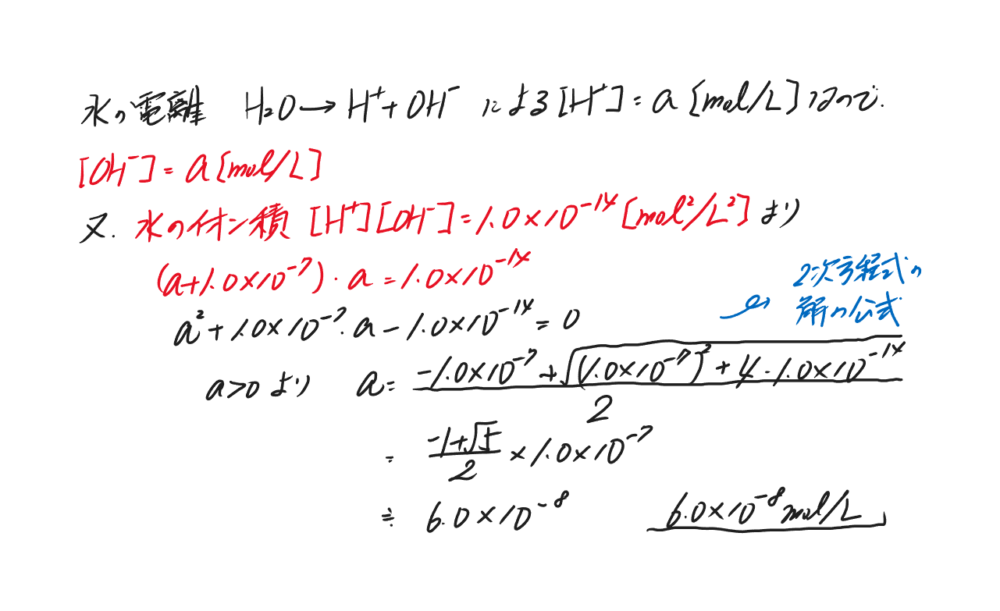- カテゴリ
まずは、前回の化学(化学平衡)の解説から!
前回の問題 化学(化学平衡)
<問題>
|
1.0×10-5mol/Lの塩酸中では、水の電離で生じた水素イオン濃度は無視して良いが、100倍希釈した1.0×10-7mol/Lでは無視できなくなる。1.0×10-7mol/Lの塩酸中の塩化水素の電離で生じた水素イオン濃度は1.0×10-7mol/Lであり、水の電離で生じた水素イオン濃度をa[mol/L]とすると、全水素イオン濃度は(a+1.0×10-7)mol/Lである。25℃における水のイオン積は1.0×10-14mol2/L2であることを用いて、25℃でのaの値を求めよ。但し、√2、√3、√5の値はそれぞれ1.4、1.7、2.2とする。 |
<ヒント>
水の電離により、水酸化物イオンもa[mol/L]だけ電離することも忘れないでくだい。
<解答>
電離平衡、化学平衡、溶解度積の問題は、質量作用の法則の式を使って解きますが、各々のイオン濃度をしっかりと考えることが肝要です。
今週の問題 数学(三角比)
<問題>
|
⊿ABCにおいて、AB=1,BC=2,CA=xとする。∠Cを最大にするxの値とそのときの最大値を求めよ。 |
<ヒント>
まずは余弦定理でcosCを表しましょう。
学習や進路に対する質問等は、お気軽に問い合わせフォームからどうぞ。お待ちしています。
お問い合わせはこちら